Torno a scrivere di JUNO e anche questa volta lo faccio a causa di un hold. Lo faccio perché in molti mi hanno contattato chiedendomi se le disgrazie di JUNO possono riflettersi su Celyad.
Cosa è successo? Come anticipato anche questa volta raccontiamo di pazienti morti durante un trial di JCAR015, dopo che per lo stesso motivo a JUNO era stato imposto un clinical hold pochi mesi fa (il terzo, in totale). Qui la scelta di fermare lo studio è volontaria ed è stata resa pubblica ieri (vi sto scrivendo nel giorno del ringraziamento), quando la compagnia ha annunciato la morte di un paziente per edema cerebrale e le condizioni disperate di un secondo che, purtroppo, è morto subito dopo il rilascio della notizia.
Tre sono gli aspetti chiave in questo caso: quanto è sicura la piattaforma di JUNO? E’ stata una mossa saggia levare il secondo hold così velocemente? Terzo aspetto, che in parte si ricollega agli altri due: il timore che ci siano più rischi che benefici impiegando linfociti ingegnerizzati si può estendere anche ad altre compagnie?
CAR-T, un minimo di background.
L’impiego di linfociti T ingegnerizzati con recettori diretti contro antigeni tumorali (CAR-T) non è esattamente una novità in ambito scientifico, ma l’impiego estensivo in clinica e le implicazioni dal punto di vista dell’investimento in titoli biotech invece si. Tramite l’impiego di vettori retrovirali o lentivirali è possibile modificare il linfocita T aggiungendo recettori chimerici per un particolare antigene (CAR). A differenza dei TCR questi costrutti hanno come target bersagli presenti sulla membrana delle cellule, quindi spesso troverete come target antigeni conosciuti, come ad esempio CD19: gli stessi impiegati dagli anticorpi monoclonali, ad esempio. Il fatto di essere linfociti con un target aggiunto ha fatto si che molti, me compreso, accostino le terapie basate su CAR-T ad anticorpi bispecifici, laddove questi ultimi abbiano uno dei due target impostato sulle cellule del sistema immunitario, come ad esempio CD3. Tanto per non far nomi, blinatumomab o AFM11 hanno come target CD3 e CD19: da una parte si legano al linfocita, dall’altra alla cellula tumorale che esprime CD19. Come facilmente intuirete è, in estrema sintesi, lo stesso principio che fa funzionare una terapia CAR-T con target CD19.
I CAR-T di prima generazione avevano una limitata attività in vivo, così, nella seconda generazione, si è provveduto ad aggiungere domini costimolatori. Nel caso ve lo stiate chiedendo, quello di JCAR015 è CD28, lo stesso di KTE-C19 di Kite ($KITE). La combinazione di multipli domini di segnale (come ad esempio CD3z-CD28-41BB), ha permesso in tempi recenti lo sviluppo di CAR-T di terza generazione che presentano cellule con una maggiore capacità di produzione di citochine e di espansione. Detta così sembrerebbe una situazione idilliaca, ma come ben sapete c’è un sinistro rovescio della medaglia: un’elevata incidenza di effetti collaterali seri, come la possibile comparsa della sindrome da rilascio di citochine (CRS), linfocitopenia e l’insorgenza di edema cerebrale, come nel caso di cui si parla oggi.
Come limitare questi effetti collaterali così pericolosi? Una scelta piuttosto intelligente è quella di proporre linfociti che abbiano, in aggiunta a quanto detto finora, anche un meccanismo di switch off, di suicidio cellulare. Due esempi? Molmed lo ha fatto con il CAR-T anti-CD44v6 (ed ha il vantaggio di avere una terapia già approvata, Zalmoxis, che impiega proprio questo meccanismo) e Bellicum ($BLCM) ha una propria piattaforma dedicata allo scopo, che probabilmente impiega il più elegante e ragionevole dei sistemi di sicurezza. In buona sostanza i linfociti ingegnerizzati vengono eliminati semplicemente somministrando un farmaco che induce il suicidio di queste cellule, qualora si presentassero eventi di una certa gravità.
Questo meccanismo avrebbe salvato i pazienti nei trial di JUNO? Il mondo crede di si, io non sono del tutto convinto, ma se dovessi puntare un euro probabilmente lo farei schierandomi dalla parte della schiacciante maggioranza.
Non c’è due senza tre (hold).
Tre stop per un farmaco sono una serie che difficilmente ha riscontri storici, se si considera il breve intervallo di tempo ne quale si sono verificati. In aggiunta alla situazione disperata di JCAR015 va anche sottolineata la fretta eccessiva con la quale FDA ha rimosso i precedenti hold (un mese per il primo, meno di una settimana per il secondo). Il terzo stop sarà quello che metterà la parola fine a JCAR015? Probabile, ma il discorso ora è più ampio. Poco tempo fa scrivevo di Adaptimmune ($ADAP) e dei rischi che avrebbe corso nel modificare lo studio clinico che vede il loro costrutto (in questo caso si parla di TCR, non di CAR-T) impiegato nel trattamento del sarcoma sinoviale. Riporto qui parte del discorso:
Ad ESMO16 Adaptimmune presenta i dati aggiornati del programma di TCR anti NY-ESO-1. […] Lo studio prevede che pazienti affetti da sarcoma sinoviale siano trattati con la terapia di Adaptimmune previa inclusione in differenti coorti. Dai dati ricavati dai primi gruppi Adaptimmune ha maturato la convinzione che un condizionamento con fludarabina e ciclofosfamide sia necessario per ottenere risposte soddisfacenti alle cellule ingegnerizzate dalla compagnia. E qui iniziano i problemi.
“Based on our clinical experience to date, we have amended the protocol for this trial to include both fludarabine and cyclophosphamide in the conditioning regimen,” Rafael Amado, CMO di Adaptimmune.
Ora, JUNO (ma non solo) insegna che l’aggiunta di fludarabina può essere un enorme problema per la sicurezza dei pazienti, avendo riscontrato casi di morte per edema cerebrale in tre pazienti sottoposti a condizionamento con fludarabina e ciclofosfamide nel trial JCAR015 (senza contare un quarto decesso in un altro studio condotto da JUNO, sempre con fludarabina presente). JUNO se l’è cavata con un hold da parte di FDA rimosso in fretta, proprio grazie all’eliminazione della fludarabina dal protocollo del trial.
A luglio JUNO se la cavò dando la colpa al condizionamento dei pazienti con fludarabina, e lo studio riprese dopo soli 5 giorni da che fu imposto l’hold. Da allora 12 pazienti sono stati trattati con JCAR015 e 2 di questi sono morti. Ovviamente la colpa non era del condizionamento.
Ora probabilmente vi starete chiedendo: ma se il problema non è il condizionamento, di cosa si tratta? E Adaptimmune come ne esce alla luce di questa svolta?
Credo sia lecito ipotizzare che il problema di JCAR015 sia proprio JCAR015. La mia posizione sul TCR di Adaptimmune al momento non cambia, anche loro hanno i loro problemi, resta da stabilire quali implicazioni ci saranno per le altre compagnie che si occupano di CAR-T. Va detto però che chi ha scelto di optare per una una linfodeplezione con fludarabina aveva assolutamente ragione nel farlo, alla luce della situazione odierna.
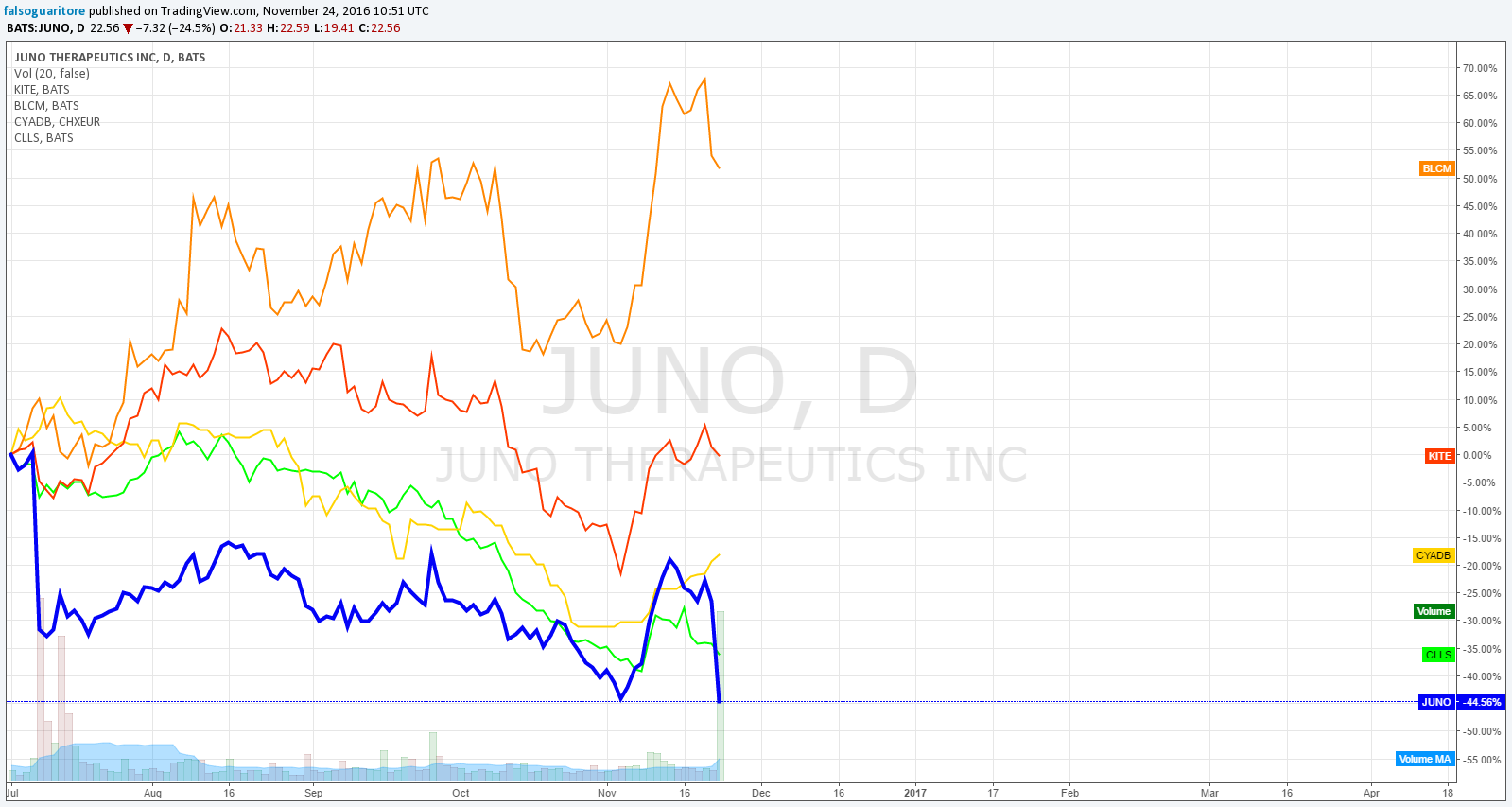
Quindi nessuna conseguenza per le altre compagnie? Non proprio, ma stiamo facendo oggi un discorso diverso rispetto a quanto fatto questa estate per il secondo hold di JCAR015. Guardate il grafico qui sotto, mostra l’andamento in borsa di alcune compagnie interessate dopo che FDA ha imposto il fermo a JUNO, per poi revocarlo pochi giorni dopo:
In prima battuta verrebbe da dire che chi ha un sistema di switch dovrebbe guadagnare dalle disgrazie di JUNO. Bellicum, infatti, ha reagito meglio dopo il secondo hold di JUNO, come si evince dal grafico. In questo caso mi aspetto che l’effetto sia più attenuato.
Molmed, Cellectis ($ALCLS) e Ziopharm ($ZIOP) hanno le loro strategie per mitigare il rischio di eventi avversi di particolare gravità ed anche JUNO impiega un meccanismo di switch off (in JCAR014 ad esempio). In buona sostanza sappiamo bene che alcune compagnie sono più attrezzate di altre ed il brutto colpo accusato da JUNO non dovrebbe avere particolari riflessi sulla concorrenza, se non, forse, su Kite ($KITE).
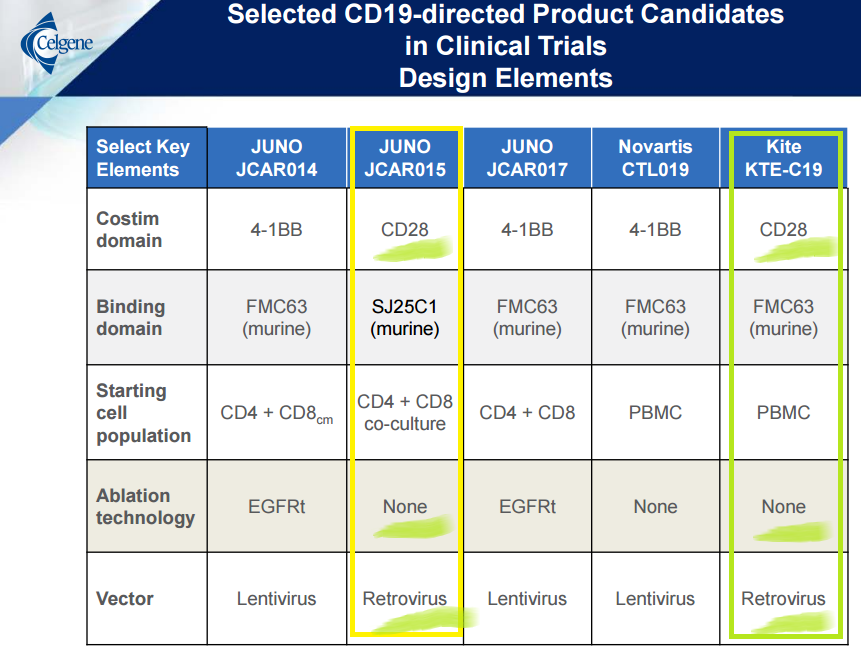
Guardate la tabella sottostante, sintetizza le caratteristiche ci alcuni CAR-T anti-CD19:
KTE-C19 non ha lo stesso costrutto di JCAR015, ma alcuni punti in comune ci sono (tutte le sottolineature sono opera mia) . Kite punta a presentarsi davanti ad FDA ad inizio 2017 e si troverà di fronte un interlocutore con la paura di approvare una terapia potenzialmente pericolosa, dopo aver commesso l’errore madornale di concedere la ripresa dello studio di JUNO dopo soli 5 giorni dal fermo, con la conseguenza tragica che stiamo raccontando oggi.
KTE-C19, va detto, non ha mai avuto problemi equipollenti a quelli che hanno attanagliato JCAR015, sia chiaro, ma FDA probabilmente sarà ipercritica nei suoi confronti.
JUNO adesso e Celyad.
Per come la vedo io, anche se seguo JUNO solo da lontano, la compagnia ora dovrebbe cancellare JCAR015, fare molta autocritica e valutare la possibilità di far avanzare JCAR017. Come potete vedere dall’immagine che vi ho proposto qui sopra i due costrutti sono completamente differenti e l’impiego di CD137 come dominio di costimolazione dovrebbe garantire una espansione delle cellule meno impetuosa, quindi più semplice da gestire anche nello sfortunato caso in cui qualcosa vada storto.
Chiaramente questo comporterà scavare un solco ancora più profondo fra JUNO e la coppia Kite e Novartis che, per rimanere in tema di CAR-T anti-CD19 si troverebbero con più di un anno di vantaggio, ma questo sarebbe il meno. Il problema di JUNO è ora quello di spiegare al mercato, e a loro stessi, per quale motivo JCAR015 ha ucciso così tante persone. Non ho motivo di dubitare che ci riescano, c’è da chiedersi: qualcuno ci crederà ancora?
Veniamo al nocciolo della questione, quello che molti mi hanno chiesto è: c’è pericolo di contagio per la quotazione di Celyad?
Premesso che l’investimento fatto in Celyad al momento è puramente finalizzato ad ASH e quindi il problema potrebbe essere relativo, colgo l’occasione per dire qualcosina sulla compagnia, visto che molti di voi hanno aperto una posizione dopo il mio ultimo report.
Celyad ha un approccio piuttosto unico al problema sicurezza del suo CAR-T più avanzato, cioè quello di cui si parlerà ad ASH, ma iniziamo con il dare uno sguardo alla pipeline immuno-oncologica:
Basta un primo sguardo per rendersi conto di un elemento importante: Celyad sviluppa CAR-T partendo da cellule del paziente, ma ha anche una piattaforma basata su un approccio off the shelf, come Cellectis. Ve ne parlerò in un’altra occasione poiché non è strettamente legato alla tesi di investimento, ma fra Celyad e Cellectis non scorre buon sangue ed il motivo riguarda proprio certe proprietà intellettuali della piattaforma della biotech belga.
Altro fattore che rende Celyad appetibile è che rivolge le proprie attenzioni ad un settore che finora le terapie CAR-T non hanno saputo affrontare: i tumori solidi. Poter competere in quel mercato significa aumentare a dismisura le possibilità di guadagno e smarcarsi decisamente rispetto alla concorrenza. La strada è decisamente in salita, su questo si deve essere chiari, ma al momento Celyad si trova in vantaggio, se non altro in termini di tempistica. Che io sappia, solo Bellicum ha in corso un trial su tumori solidi: un costrutto anti-PSCA nel trattamento del tumore del pancreas in fase 1.
Ultimo aspetto interessante, motivo per il quale ho sostenuto che i guai di JUNO non avrebbero intaccato Celyad è legato alla sicurezza della terapia: laddove la maggior parte delle altre concorrenti fa sfoggio della permanenza delle cellule modificate nel paziente, Celyad sceglie l’approccio contrario: la terapia viene infusa, agisce e toglie il disturbo. Devo ammettere che questo è uno degli aspetti che mi lascia più perplesso, al momento, tuttavia, sembra che ci siano già interessanti cenni di attività ed il profilo di sicurezza sembra rassicurante.
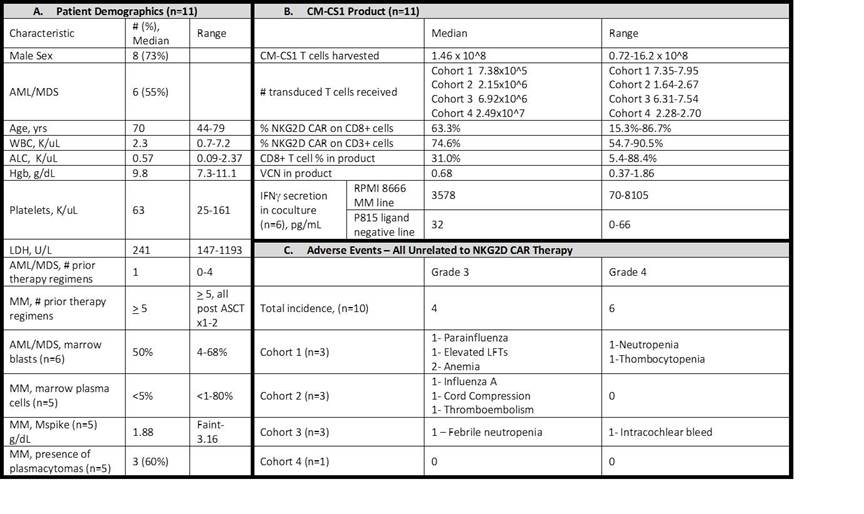
Nella tabella qui sopra trovate alcuni dati racchiusi nell’abstract presentato recentemente per ASH, sintetizzano le caratteristiche dei pazienti arruolati e dei trattamenti subiti. Si sono verificati alcuni eventi avversi di grado 4 ma sembrano legati al decorso delle malattie piuttosto che alla terapia di Celyad. Il numero di pazienti è ridotto, quindi difficile trarre conclusioni, però va detto che la mancata permanenza delle cellule (elemento positivo in questo caso) si è manifestata in tutti i pazienti, tranne uno. Chiaramente avrei preferito che le cellule non venissero riscontrate in nessun paziente.
Conclusione.
Seguo Celyad fin da quando si occupava (male) di malattie cardiovascolari. Ad un certo punto della loro esistenza hanno capito che puntare dritto in quella direzione era una scelta piuttosto rischiosa e, pur continuando a lucidare maniglie sul Titanic, hanno deciso di cambiare nome ed hanno improntato un piano B da seguire in caso fosse il caso di buttare in acqua le scialuppe di salvataggio in fretta. Devo aggiungere però che senza l’intervento di Massimo e di un altro oscuro personaggio probabilmente avrei lasciato la compagnia (quasi) ferma ai box. Sarebbe stato un peccato, alla luce delle quotazioni recenti, quindi li ringrazio. Dovessero andar male le cose, alla fine, sappiate che è tutta colpa loro e che non mi sono mai fidato!
Scherzi a parte Celyad al momento rimane una storia legata al prossimo ASH, ma ha il potenziale per essere un buon investimento nel lungo periodo. Deciderò in corso d’opera.

@Tarantella, non saprei, in linea di massima non credo possano aggiungere molto altro rispetto a quanto emerso finora.
@LSW, io aggiungerei a quanto giustamente dici che in AML si sono viste cose interessanti. Una delle vincitrici secondo me è $SGEN… una grande compagnia che, tra l’altro, potrebbe far bene anche al SABCS. Oh, detto questo, si, sto scrivendo due righe su ASH16…
CK da CYAD domani può uscire qualcosa in più di positivo o… negativo? Non si è mossa molto oggi purtroppo
@Lucaluca, l’accordo migliore (sempre) include un sostanzioso pagamento in upfront. nel caso di $MLM non ci sono termini finanziari quindi difficile esprimersi ma, in linea di massima, è un ulteriore passo verso la commercializzazione di Zalmoxis e per certo, vista la nulla esperienza nel campo, meno è coinvolta Molmed e meglio è. ad ognuno il proprio mestiere 😉
http://www.trend-online.com/ansa/molmed-e-megapharm-siglano-un-term-sheet-per-la-commercializzazione-di-zalmoxis-in-israele-257444/
Salve a tutti buon accordo per molmed in Israele?
grazie
@Alex, di nulla ed il bocca al CD47… adesso sto scrivendo di $BLUE, poi magari due righe su $TRIL…
@Maurizio, $NKTR mi è sempre piaciuta ed ala luce della maxi emissione di qualche settimana fa sembra sempre più appetibile. il cd122 agonista (non ricordo il nome al momento…) potrebbe essere un bonus decisamente interessante.
$ADMS non la conosco; $ALDR la seguo poco perché detesto chi si occupa di emicrania. L’approccio di $ADLR è tuttavia interessante e credo abbiano un evento importantissimo già in 1h17 (fase 3 dell’anti-anti-CGRP per il trattamento dell’emicrania) anche se non conosco le tempistiche esatte. potrebbe essere un buon investimento in ottica binaria, di certo hanno cassa ed evento. a parer mio capitalizza ancora un po’ troppo (oltre 1B$) ma se scendesse bene…
Grazie della risposta CK. Non essendo tanto esposto penso di tenerle anch’io.
Ciao cosa ne pensi di aldr, nktr ed adms?
Grazie
@Lsw, $CYAD? la tesi d’investimento per ASH rimane in piedi, l’unico intoppo che potrebbe aver causato la discesa, prese di beneficio a parte, è qualche notizia circa le proprietà intellettuali e la contesa con $ALCLS, ma non vedo nulla a riguardo…
@Alex, non posso darti un consiglio specifico perché non conosco la tua situazione. io, comunque, le tengo. Il rischio per me adesso è relativo, vista la scarsa esposizione che ho sul titolo. una volta valutati i dati che presenteranno ad ASH potrei anche incrementare, di certo ci sarà tempo per farlo, se ne varrà la pena.
Ciao CK. Sono seriamente combattuto tra liquidare TRIL domani o attendere lunedì o martedì. Tu cosa faresti?
Mhhh , giornatina di M pure oggi.. speriamo sia solo una scrillatina prima della ripartenza era salita di un 40% dai minimi … 😰
@Lsw, mi pare che si stiano allineando 🙁
@Marco, grazie. Evotec è rock solid!
https://uk.finance.yahoo.com/news/evotec-merck-enter-agreements-collaborate-073200065.html
CYAD in Eu scende , in Usa sale … al cambio dovrebbe essere sui 22 euro , invece è a 18,90 . 🤔 Vediamo oggi certo che sto ADR scambia niente e va dove vuole !!!
ck…ontx 🙁
Cereal hai mai preso in considerazione un entrata su Bellicum ?
Oggi non bella giornata per CYAD , piccolo sell off 🤔
@Marco, grazie!
http://finance.yahoo.com/news/trillium-therapeutics-announces-conference-call-120000220.html
@Gian, desumi correttamente. Molmed ha il vantaggio non trascurabile di avere un meccanismo di switch off già approvato ed un target poco battuto. Per contro è indietro in termini temporali, ma se si muoveranno con sensatezza (al contrario di quanto fatto con NGR) potranno recuperare lo svantaggio.
Ciao CK …in conclusione desumo che anche la tanto tartassata Molmed ne esca avvantaggiata da tutta questa vicenda…o no? 🙂