Ho già avuto modo di parlarvi di GTx in passato, anche grazie al fatto che il titolo ha attraversato con profitto il portafoglio virtuale. Il motivo del mio interesse nella compagnia risiede in Ostarine, noto anche come Enobosarm. Il farmaco, ha il compito di combattere la cachessia in soggetti affetti da tumore, ossia la perdita di peso e massa muscolare, complicazioni severe che sono normalmente causate dal cancro. Ostarine, si trova ora in due distinte fasi 3 che daranno esito a dati presumibilmente verso giugno:
“More than 600 patients in the United States, Eastern Europe and South America are now participating in our two definitive Phase III clinical studies of enobosarm,” said Mitchell Steiner, MD, CEO of GTx. “After the last patient completes each of the five month studies, we expect to receive top line data during the latter part of our second quarter in 2013. We are excited about the potential of enobosarm to prevent and treat muscle wasting in patients suffering from non-small cell lung cancer.”
Eravamo a dicembre quando GTx lo ha comunicato. Nel frattempo GTx ha portato a casa la fast track da FDA, fatto che consentirà alla compagnia di accelerare il processo di revisione della domanda di autorizzazione, il che spesso si traduce anche in maggiori possibilità di ottenere una priority review.
Il nocciolo del discorso è questo, può il contrastare la cachessia tradursi in un miglioramento dal punto di vista della sopravvivenza in pazienti affetti da cancro? La risposta sembrerebbe essere: si. La seconda domanda dovrebbe quindi essere: lo può fare Ostarine?
GTx, un partner l’aveva…
GTx non è l’unica compagnia a perseguire lo scopo di contrastare la cachessia in pazienti affetti da tumore. La lista è anche abbastanza lunga e molti dei nomi in essa contenuti hanno un minimo comune denominatore: la mancanza di partner di peso. La svizzera Helsinn ad esempio sta arruolando in 3 studi registrativi (ROMANA 1,2 e 3) che vedono impiegato Anamorelin, un agonista della grelina, un ormone in grado di stimolare l’appetito e la produzione dell’ormone della crescita. Nota a parte, esistono due forme di grelina e come recentemente dimostrato anche da uno studio italiano condotto anche grazie ai fondi di Telethon, sembrerebbe che la più trascurata delle due abbia un notevole potenziale nel combattere la cachessia. Tornando a noi, Helsinn ha recentemente siglato un accordo con Stendhal che però non fa gridare al miracolo e riguarda solo il centro America. Date uno sguardo alla seguente tabella:
| Selezione di farmaci in fase di sviluppo per il trattamento della cachessia legata a tumori. | ||||
| Compagnia | Farmaco | Fase | Meccanismo o tipo di farmaco | Note |
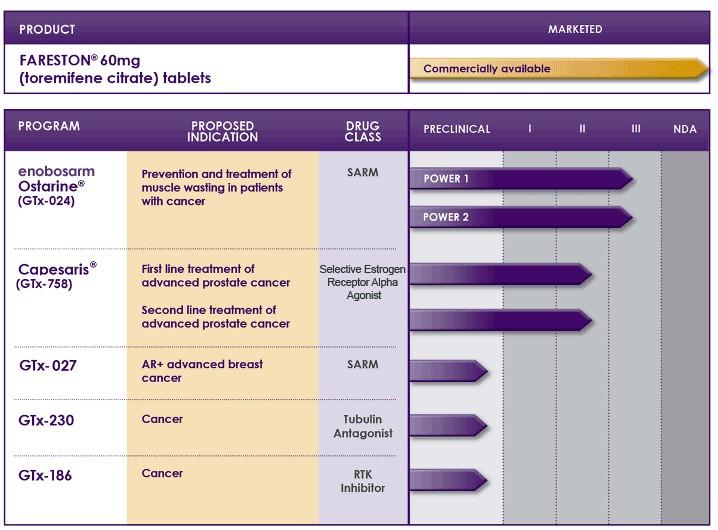
| Gtx | Ostarine | 3 | SARM | POWER 1 e 2 sono studi registrativi, i dati dovrebbero essere disponibili per fine 2Q13 |
| PsiOxus Therapeutics | MT 102 | 2 | Agente di Trasformazione Catabolico Anabolico | Sta reclutando in fase 2; uno studio multicentrico randomizzato, in doppio cieco vs placebo a diversi dosaggi di MT 102 in 132 sogetti con cachessia e NSCLC di grado III e IV o cancro al colon. I dati erano attesi per il 2012 ma l’arruolamento risulta ancora aperto all’ultima verifica. |
| Helsinn | Anamorelin | 3 | Agonista della grelina | Tre fasi 3 (ROMANA 1,2 e 3) e stanno tutte ancora arruolando. |
| Ohr Pharmaceuticals | OHR/AVR118 | 2 | Fase 2 open label in pazienti con diverse forme di tumore in fase avanzata, ha concluso l’arruolamento di 20 pazienti. | |
| Xbiotech | MABp1 | IL-1α antagonista | Sta per iniziare una fase 3 negli USA, il primo paziente dovrebbe essere arruolato in 1Q13. Lo studio si rivolge a pazienti con cancro al colon-retto. | |
| Alder/Bristol Myers Squibb | ALD 518 | 2 | IL-6 antagonista | Attualmente in fase di sviluppo per Morbo di Crohn. |
| Morphosys/Novartis | BYM 338 | 2 | ACT RIIB | In fase 2 sia in pazienti con perdita di peso e cancro al pancreas sia in pazienti affetti da sarcopenia. Probabile l’inizio di una fase 3 nel 2013. |
| Acacia Pharma | APD 209 | 2 | Megestrol e Formoterol | Nuova formulazione di due farmaci esistenti ad un dosaggio prefissato. Megestrol viene attualmente impiegato offlabel per il trattamento della cachessia. |
| Aeterna Zentaris | AEZS 130 | 2 | Agonista della grelina | In fase 2 , doppio cieco vs placebo in pazienti con cachessia e differenti forme di tumore solido. Lo studio sta ancora arruolando pazienti, il target è di 26 soggetti. |
| Vicus Therapeutics | VT 122 | 2 | In fase 1il 50% dei soggetti trattati con VT 122 ha mostrato un aumento statisticamente significativo di almeno il 5% di massa corporea dopo 12 settimane di trattamento contro lo 0% del controllo. Vicus sta anche arruolando in fase 2 pazienti con carcinoma epatocellulare ed a rischio cachessia ai quali viene somministrato VT 122 in combo con Sorafenib. Lo scopo del trial è misurare la differenza in termini di mortalità rispetto al solo sorafenib. | |
Ora, di tutti questi farmaci elencati in tabella, BYM 338 di Morphosys (MOR) sembra il più serio pretendente al trono proprio in virtù della partnership con Novartis che pare essere interessata a portare il progetto in fase 3, qualora i dati forniscano speranza di successo.
Il mercato potenziale per GTx è elevato e la velocità con la quale hanno arruolato i pazienti è confortante e dice molto dell’interesse per il composto. Ripeto qui quanto già detto nel precedente articolo: GTx aveva un partner, Merck, che ha mollato il colpo. Ai tempi Ostarine era investigato più sul versante sarcopenia legata all’invecchiamento, ma già una fase 2 nel trattamento della cachessia legata a tumore era in corso.

Fase 2b di Ostarine nel sottogruppo di pazienti con tumore al polmone (NSCLC), si notano i miglioramenti sia in termini di massa che in termini di funzionalità dei muscoli.
Niente partner può significare un rischio elevato, ma i motivi per essere ottimisti ci sono e riguardano i dati che GTx ha finora accumulato oltre all’evidenza che non perdere massa muscolare influisce positivamente anche in termini di sopravvivenza dei pazienti, oltre che in termini di qualità della vita. Un analisi relativa alla fase 2b ha mostrato che in pazienti con NSCLC (tumore al polmone) una perdita di massa maggiore dell’8% la sopravvivenza è inferiore rispetto a quanti abbiano sperimentato una perdita di massa corporea inferiore (p value 0,04) mentre nella popolazione ITT, che comprendeva anche casi di linfoma e altri tumori solidi, lo stesso fenomeno si verificava ed il dato era ancora più significativo statisticamente parlando: p value 0,003. La cosa interessante però è che tale fenomeno, ossia un aumento della mortalità nei pazienti con maggior perdita di indice di massa corporea non si verificava nei pazienti trattati con il farmaco di GTx.
GTx, in conclusione…
Secondo me merita un investimento binario per sfruttare l’attesa dei dati.
At September 30, 2012, GTx had cash and short-term investments of $47.3 million and in October 2012, GTx increased its cash and short-term investments when it received net cash proceeds of approximately $19 million from the sale of FARESTON®.
Cassa quindi ce n’è abbastanza, anche se il rischio se il titolo dovesse salire ancora ci può essere.
Grazie Gooser, giornata piena oggi, vediamo se riesco a scrivere anche di Celsion…
Celsion Corporation (NASDAQ: CLSN), a leading oncology drug development company, today announced that ThermoDox® in combination with radiofrequency ablation (RFA) did not meet the primary endpoint of the Phase III HEAT Study in patients with hepatocellular carcinoma (HCC), also known as primary liver cancer.
Specifically, Celsion has determined, after conferring with its independent Data Monitoring Committee (DMC) that the HEAT Study did not meet the goal of demonstrating persuasive evidence of clinical effectiveness that could form the basis for regulatory approval in the population chosen for study. The HEAT Study was designed to show a 33% improvement in PFS with 80% power and a p-value = 0.05. In the trial, ThermoDox® was well-tolerated with no unexpected serious adverse events. The HEAT Study was conducted under a Special Protocol Assessment agreed to with the U.S. Food and Drug Administration (FDA).
“We are disappointed that the HEAT Study did not provide sufficient evidence of clinical effectiveness of ThermoDox® as measured by the trial’s primary endpoint,” said Michael H. Tardugno, Celsion’s President and Chief Executive Officer. “We will consider following the patients currently enrolled in the HEAT Study to the secondary endpoint, Overall Survival (OS), and are conducting additional analyses of the data from the trial in order to assess the future strategic value of ThermoDox. We expect that the results will be presented in the future at appropriate medical meetings. We wish to acknowledge and thank the patients and investigators who participated in the trial.”
Celsion ended 2012 with a strong balance sheet that provides the Company the opportunity to evaluate its future development plans. The Company projects its unaudited cash and investment balance to be approximately $23 million as of December 31, 2012 and approximately $27 million as of January 31, 2013.
E dopo questa… 😉
Cosa volete che cachesSIA?